胆囊癌(Gallbladder cancer,GBC)是一种罕见但致命性极高的恶性肿瘤,患者普遍预后极差。长期以来,由于缺乏对其发病基础和生物学背景的认识,临床治疗手段仍十分有限。特别是胆囊癌极高的遗传异质性,使得基于基因组突变的靶向治疗在临床上难以取得突破。然而,越来越多的证据表明,表观遗传失调在胆囊癌的发生和发展中起着关键作用。尽管既往研究多聚焦于非编码RNA和基因启动子甲基化的变化,其他表观遗传领域的机制研究仍存在诸多空白。
超级增强子(Super Enhancer, SE)是一类近年来发现的重要表观遗传调控元件,由谱系特异性核心转录调控网络(Core Regulatory Circuitry, CRC)驱动,其重编程可引发癌症中转录失调。因此,系统解析胆囊癌中的超级增强子分布和功能,并阐明胆囊癌核心转录调控环路,以及它们对表观遗传靶向药物的敏感性,不仅可以帮助深入剖析胆囊癌发生及存活的致病分子机制,还能为个性化分子诊断与靶向治疗提供全新思路。
近日,上海交通大学医学院附属仁济医院刘颖斌教授、唐玉杰教授团队联合浙江大学王超尘教授团队在 Advanced Science 发表题为 “Super-Enhancer Reprogramming Driven by SOX9 and TCF7L2 Represents Transcription-Targeted Therapeutic Vulnerability for Treating Gallbladder Cancer” 的研究论文。该研究首次构建了胆囊癌超级增强子图谱,揭示了 SOX9-TCF7L2核心转录调控网络在胆囊癌超级增强子重编程中的关键作用,并通过单细胞转录组分析进一步阐明其作为分子标记的潜在临床价值。这项研究为胆囊癌的预后分层和个性化治疗策略的开发提供了重要依据。
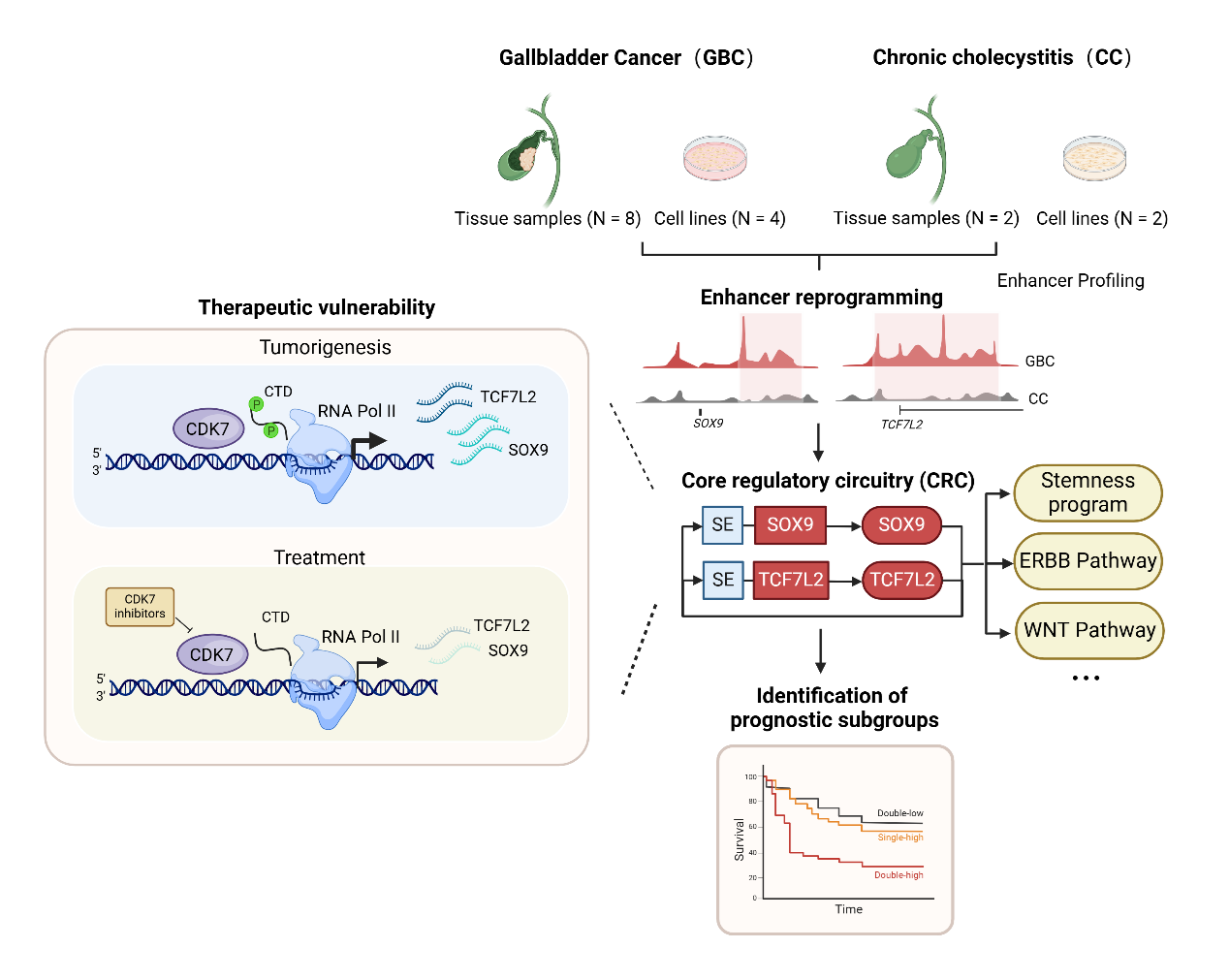
研究团队利用染色质靶向酶切测序(CUT&Tag)和染色质免疫共沉淀测序(ChIP-seq),在10例新鲜冷冻组织和细胞系样本中分析了活性转录标记组蛋白修饰H3K27ac的分布情况。结果表明,GBC样本与良性胆囊病变(chronic cholecystitis, CC)样本中超级增强子分布存在显著差异,揭示了胆囊癌发生过程中超级增强子的重编程现象。具体而言,研究共鉴定出820个GBC特异性超级增强子(GBC-specific SEs)和369个CC特异性超级增强子(CC-specific SEs)。进一步功能富集分析显示,GBC-specific SEs 的靶基因主要富集于 TGFβ、EGFR、MAPK 和脂代谢等已知致癌信号通路,而 CC-specific SEs 的靶基因主要参与正常胆囊功能。此外,GBC-specific SEs 靶基因在胆囊癌样本中的 mRNA 表达水平显著高于 CC-specific SEs 靶基因。
为了识别主导GBC中SE重编程的核心转录因子(CRC TF),研究利用“Coltron”算法分析了GBC与对照样本的SE图谱,共鉴定出43个候选核心转录因子(CRC TF)。结合DepMap全基因组CRISPR筛选数据、GBC RNA-seq数据及Coltron预测结果,研究评估了这些候选CRC TF的基因表达和肿瘤依赖性水平。通过Pearson相关性分析和GBC细胞模型验证,发现SOX9和TCF7L2在GBC中高度共表达,且两者之间存在相互转录依赖性——敲低其中一个会显著降低另一个的mRNA水平。进一步的网络分析表明,SOX9和TCF7L2在胆囊癌转录网络中处于核心地位,构成了一个SE驱动CRC。
随后,通过体外和体内实验,研究验证了SOX9和TCF7L2对于维持GBC恶性表型的必要性。敲低这两个转录因子可显著抑制GBC细胞增殖和肿瘤生长。此外,结合TF CUT&Tag、Hi-C数据和CRISPR干扰系统,研究证实SOX9与TCF7L2之间存在直接的转录自调控及共调控关系。进一步分析发现,该CRC通过占据GBC-specific SE,共同调控胆囊癌特异的发育谱系特征和恶性基因表达特征。
单细胞转录组分析显示,SOX9-TCF7L2高表达的肿瘤细胞富集了GBC-specific SE基因特征,并与更差的患者预后显著相关。在扩大的胆囊癌临床队列(n=106)中,通过免疫组化(IHC)分析,研究进一步验证了SOX9和TCF7L2的高表达与较差的总生存期(OS,p=0.019)和无复发生存期(RFS,p=0.057)显著相关,提示SOX9-TCF7L2的表达水平可用于定义具有临床意义的肿瘤亚群。研究进一步发现,SOX9-TCF7L2高表达的胆囊癌模型对SE靶向CDK7抑制剂表现出显著敏感性。SE驱动的转录依赖性为胆囊癌的精准治疗提供了新的靶点。这一发现为预后较差的胆囊癌患者开辟了一条潜在的治疗路径,也为表观遗传药物的临床应用奠定了基础。
综上所述,本研究首次揭示了胆囊癌中超级增强子的重编程机制及其调控网络SOX9-TCF7L2 CRC的关键作用。这项工作不仅加深了对胆囊癌发病机制的理解,还为其预后分层和个性化治疗策略的开发提供了重要支持。未来,这一发现有望推动表观遗传靶向药物在胆囊癌中的临床应用,助力攻克这一致命性肿瘤的治疗难题。
上海交通大学医学院附属仁济医院刘颖斌教授,组织胚胎学与遗传发育学系唐玉杰研究员与浙江大学癌症研究院王超尘研究员为该论文共同通讯作者。严思远博士,博士生刘照南,博士后隋怡(上海交通大学)和博士生王腾(浙江大学)为共同第一作者。该研究有幸得到了海军军医大学第三附属医院姜小清教授和冯飞灵教授的帮助。
上海交通大学医学院附属仁济医院胆胰外科主任、上海市肿瘤系统调控与转化重点实验室(筹)主任刘颖斌教授团队,多年来致力于BTCs的临床和基础研究,其系列研究成果覆盖BTCs的临床流行病学研究、发生发展机制研究、早期诊断研究、综合治疗和转化医学研究等多个领域,在国内外具有较高的影响力。上海交通大学医学院组织胚胎学与遗传发育学系唐玉杰研究员团队长期致力于恶性肿瘤的表观遗传学研究,以第一/共同第一作者或通讯/共同通讯作者在Nature Medicine、Cancer Cell和PNAS等刊物发表多篇研究论文,为拓展恶性儿童脑瘤的表观遗传致病机制与靶向治疗研究方向做出了重要贡献,